某化学小组用一定量硝酸银和硝酸铝的混合溶液进行了如图实验,下列说法错误的是( )
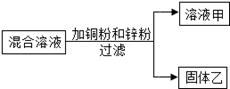
- A.若溶液甲呈蓝色,则向固体乙上滴加盐酸时没有气泡产生
- B.若溶液甲呈蓝色,则固体乙中一定没有铜
- C.若固体乙中含有锌,则溶液甲中一定没有硝酸铜
- D.若固体乙中含有铜,则溶液甲中一定没有硝酸银
答案
正确答案:B
知识点:滤液、滤渣成分确定
在金属活动性顺序里,金属的位置越靠前,它的活动性就越强;位于氢前面的金属能置换出盐酸、稀硫酸中的氢;位于前面的金属能把位于后面的金属从它们化合物的溶液里置换出来。
由金属活动性顺序可知,活动性:Al>Zn>H>Cu>Ag。向AgNO3和Al(NO3)3的混合溶液中加入Cu和Zn,Al的活动性强于Cu和Zn,故Al不会被置换出来。由金属活动性强的首先去置换金属活动性比较弱的,可知Zn首先置换Ag,故固体乙中一定含有Ag,溶液甲中一定含有Al(NO3)3和Zn(NO3)2。
A.若溶液甲呈蓝色,说明溶液甲中含有Cu(NO3)2,有Cu(NO3)2存在,就不会有比Cu活动性强的Zn剩余,故固体乙中一定不含Zn,一定含有Ag,加入的Cu是否过量无法确定。则向固体乙上滴加盐酸时没有气泡产生。A正确,B错误。
C.若固体乙中含有Zn,则Zn有剩余Cu不会参加反应,溶液甲中一定没有Cu(NO3)2。C正确。
D.若固体乙中含有Cu,则Cu有剩余,Ag全部被置换出来,则溶液甲中一定没有AgNO3。D正确。
故选B。
略








