实验室加热30gKClO3和MnO2的混合物制取O2,完全反应后剩余固体质量为20.4g,则原混合物中MnO2的质量为( )
- A.5.5g
- B.9.6g
- C.15.1g
- D.24.5g
答案
正确答案:A
知识点:化学反应方程式的计算
根据质量守恒定律,反应前后减少的质量为生成O2的质量。则生成O2的质量为:
30g-20.4 g=9.6 g。要求原混合物中MnO2的质量,只要求出原混合物中KClO3
的质量即可,由于题目中给出了“完全反应”,则KClO3全部参加反应分解为O2,
根据O2的量即可求出KClO3的质量,从而求出MnO2的质量。
设原混合物中KClO3的质量为x,则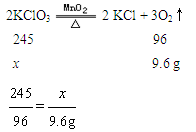
解得x=24.5g
则MnO2的质量=30 g-24.5 g=5.5 g。
故选A。
略







