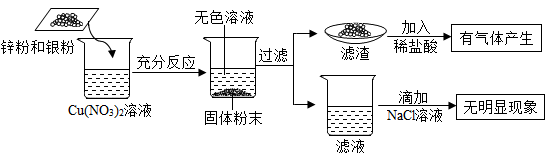
将一定质量的锌粉和银粉加入Cu(NO3)2溶液中,充分反应,实验过程及实验现象如下图所示,则下列判断中正确的是( )
- A.滤液中可能含有Ag+
- B.滤渣中可能含有单质锌
- C.滤液中一定含有Cu2+
- D.滤渣中一定含有单质铜
答案
正确答案:D
知识点:金属活动性的应用
金属与金属化合物溶液反应后,判断滤渣、滤液成分,解题步骤:①对涉及到的金属进行活动性排序,标出加入的金属;
②画流程图,初步判断滤渣、滤液成分;
③根据题中信息,再次判断滤渣、滤液成分。
题目中涉及到的金属有Zn、Ag、Cu,活动性顺序为Zn>Cu>Ag,其中加入的金属为Zn、Ag。根据金属活动性可知,Zn能够置换出溶液中的Cu,Ag不能置换出溶液中的Cu。
加入一定量的Zn后与Cu(NO3)2溶液反应置换出Cu,Zn反应后生成Zn(NO3)2,因为反应后为无色溶液,因此溶液中不含Cu(NO3)2,说明Cu全部被置换出来。因此滤渣中一定含有Cu和未参加反应的Ag,可能含有过量的Zn,滤液中只含有生成的Zn(NO3)2。向滤渣中加入稀盐酸,有气体产生,故滤渣中一定含有氢前金属,只能是Zn,故滤渣中一定含有Cu、Ag、Zn。故A、B、C错误,D正确。
故选D。
略








