某化工厂排放的废液中只含有ZnCl2和CuCl2两种溶质,为回收金属Cu并得到ZnCl2固体,化学小组的同学们设计并进行了如下实验:
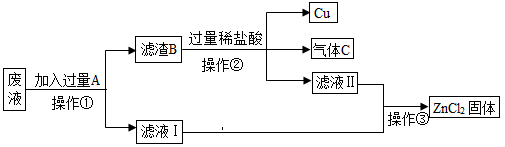
加入的金属A是____(填物质名称);滤液I中的溶质是____(填物质名称);滤渣B中含有的物质是____(填物质名称)和____(填物质名称),气体C是____(填物质名称)。
答案
锌,氯化锌,铜,锌,氢气
知识点:金属活动性的应用
废液中回收金属和金属化合物解题步骤:
根据回收目的,结合反应后滤渣、滤液成分,分析各环节的物质组成和化学反应。
题目中涉及到的金属有Zn、Cu、A,活动性顺序为Zn>Cu,其中加入的金属为A。
加入过量的A后得到滤渣B和滤液I,滤渣B中一定含有过量的金属A,滤液I能经过操作③得到ZnCl2固体,故滤液I为ZnCl2溶液。滤渣B加入过量的稀盐酸得到Cu、气体C和滤液B,Cu不与稀盐酸反应,故滤渣B中一定含有Cu,金属和稀盐酸反应生成的气体C为H2,滤液II经过操作③得到ZnCl2固体,因此滤液II为ZnCl2溶液。由上述分析已知滤渣B中含有金属A,金属A与盐酸反应得到ZnCl2溶液,故金属A为Zn。
略








