化学实验探究(一)
满分100分 答题时间20分钟
已经有446位用户完成了练习
填空题(本大题共小题, 共分)
-
1.(本小题12分)
背景:市场上销售的豆腐干、盐水鸭等食品,常采用真空包装,即将食品装入包装袋,抽出包装袋内的空气,再充入防止食品变质的气体,然后封口。真空包装的目的是除去空气使大多数微生物因缺少____(填物质名称)生命活动受到抑制,停止繁殖,从而防止食品变质。
[提出问题]充入食品包装袋中的气体是什么?
[猜想假设]同学们经过激烈讨论,最后提出了气体可能有三种情况:①N2;②CO2;③H2。
[提出方案](1)小明同学认为气体不可能是H2,因为它具有____性。
(2)为了继续探究气体的成分,小华和小红两位同学各提出了一种方案。
①小华方案:收集一瓶该气体,把一根燃着的木条伸入瓶中,发现木条熄灭。由此得出气体是CO2。该方案是否可行?____(填“是”或“否”)。
②小红的方案被同学们认可。走进食品生产工厂,在装有该气体的容器(容器内压强接近大气压)上连接了如图的装置。
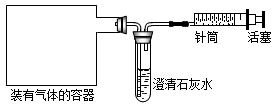
a.为了使容器内的气体通过澄清石灰水,活塞应向____(填“左”或“右”)移动。
b.不管气体是CO2还是N2,试管中都有的实验现象是导管口有____产生。
c.经过实验后,发现澄清石灰水变浑浊,证明气体是____(填物质名称)。
核心考点: 实验探究
-
2.(本小题22分)
天然气的主要成分是甲烷(CH4),化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,请你参与探究:
甲烷在氧气中燃烧后生成哪些物质?含碳元素的物质在氧气中完全燃烧生成CO2,不完全燃烧生成CO;无水CuSO4(白色)遇水变蓝色。
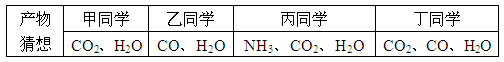
你认为____同学的猜想是错误的。为了验证上述猜想与假设,将甲烷在一定量的氧气中燃烧的产物依次通过如图装置:
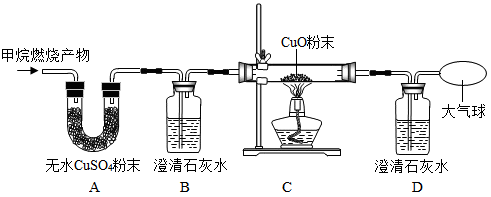
(1)A、B装置的顺序____(填“能”或“不能”)颠倒,若颠倒,将影响产物____(填物质名称)的检测。
(2)实验中用纯净氧气而不用空气的原因是空气中含有____(填物质名称)和____(填物质名称)。
(3)实验中观察到A中无水CuSO4粉末由____色变为____色,B中澄清石灰水____(填“变”或“不变”)浑浊,C中____色粉末变成光亮的____色,D中澄清石灰水____(填“变”或“不变”)浑浊,由此推断丁同学猜想成立。
核心考点: 实验探究
-
3.(本小题8分)
课本上测量空气中氧气体积分数的实验装置存在不少的缺点,如污染环境、误差较大等。小明同学在老师指导下,利用铁锈蚀原理测量空气中氧气的体积分数。
[查阅资料]脱氧剂的主要成分为铁粉、少许活性炭、少量氯化钠和水。活性炭是一种载体,可以使脱氧剂中各组分混合均匀,并使铁粉疏松、透气。
[实验原理]铁生锈消耗集气瓶中的____(填物质名称),生成固态的铁锈,使集气瓶内压强____(填“增大”或“减小”),在压强差的作用下,量筒内水进入集气瓶;氯化钠可以加快铁锈蚀的速率。
[实验过程](1)取一个集气瓶,其实际容积是150mL,取一个量筒,内盛100mL的水。
(2)室温时,将一定量的脱氧剂悬吊在橡皮塞上,再将橡皮塞旋紧到集气瓶口,然后将导气管插入量筒内(如图所示),观察现象。
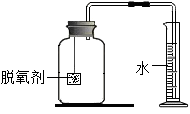
(3)当量筒内水面高度不再变化,且温度恢复至室温时,读出水面在73mL刻度处。
[实验结果]由上述实验数据可以算出,空气中氧气的体积分数是____%。
[反思拓展]本实验的测量结果与理论值不一致,原因可能是____(填字母序号)。
A.使用了足量的脱氧剂
B.脱氧剂中有部分铁粉在实验前已被氧化
C.脱氧剂中的内层的铁粉没有与氧气接触
核心考点: 实验探究
-
5.(本小题40分)
在实验探究课上,老师给同学们一包红色粉末,该粉末是铜粉和氧化铁粉末中的一种或两种。同学们为确定该粉末的成分,进行如下探究。请回答下列问题。
[查阅资料]金属氧化物能够溶于稀酸;铜不溶于稀酸。
[提出问题]红色粉末成分是什么?
[猜想假设]
猜想1:红色粉末是____(填物质名称);
猜想2:红色粉末是氧化铁;
猜想3:红色粉末是铜和____(填物质名称)的混合物。
[设计方案]取少量红色粉末放入硬质玻璃管中,____(填字母序号),充分反应并观察现象(实验装置如图所示)。
A.先通入一段时间的一氧化碳,然后再点燃酒精灯加热
B.先点燃酒精灯加热一段时间,然后再通入一氧化碳
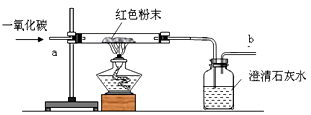
请你完成下表:

将表中需要填写的内容填写到下列横线上:
①____;②____;③____;④____;⑤____。
[实验结论]同学们进行了实验并经过分析,确认猜想3成立。
[反思评价]请你用另一种反应原理证明猜想3成立,实验方案是取少量红色粉末于试管中,加入足量的____充分反应,试管底部有____色固体剩余,溶液变为黄色,则猜想3成立。
核心考点: 实验探究









