实验室常用燃烧的方法测定有机物的组成。某有机物在足量氧气中充分燃烧,生成4.4g二氧化碳和3.6g水,关于该物质的描述正确的是( )
- A.该物质只含有碳、氢两种元素
- B.该物质中碳、氢两种元素的质量比为11:9
- C.该物质的分子中碳原子与氢原子的个数比为1:2
- D.一定含有碳、氢两种元素,可能含有氧元素
答案
正确答案:D
知识点:元素种类和质量守恒
题干给出部分组成已知的物质质量,让判断组成未知物质的相关信
息。此类题目,需根据元素的种类和质量守恒来解答。
用X表示该有机物,根据题意,该反应可表示为:
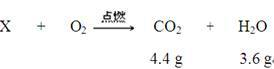
由质量守恒定律,反应前后元素的种类和质量守恒。根据元素的种类守恒,X中
一定有碳元素和氢元素,可能含有氧元素,故A错误D正确;
根据元素的质量不变,X中碳元素的质量等于4.4gCO2中碳元素的质量:
4.4 g×![]() ×100%=1.2 g
×100%=1.2 g
X中氢元素的质量等于3.6gH2O中氢元素的质量:
3.6 g×![]() ×100% = 0.4 g
×100% = 0.4 g
故碳、氢元素质量比为:1.2 g :0.4 g =3:1,故B错误;
设X分子中,碳原子与氢原子的个数分别为m、n,
根据元素质量比=(相对原子质量×原子个数)之比,则:
(12m):n=3:1,解得m:n=1:4
即该物质的分子中碳原子与氢原子的个数比为1:4,故C错误。
故选D。
略







