金属与人类的生活、生产密切相关。
(1)每年世界上钢铁的产量很高,但钢铁的锈蚀也给人类带来了巨大的损失。铁在空气中锈蚀,实际上是铁与空气中的 等物质相互作用的结果;日常生活中可采用一些防锈措施,如: 。
(2)如图是元素周期表的一格,下列说法正确的是 。
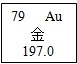
A.金元素属于非金属元素
B.金原子的中子数为197
C.金原子的核外电子数为118
D.金元素位于第六周期第IB族
(3)在研究金属的性质时,某小组同学进行了如下实验探究;将一定量铁粉加入到硫酸锌和硫酸铜的混合溶液中,充分反应后过滤,然后对滤纸上的物质进行分析和实验。
【提出问题】滤纸上的物质是什么?
【做出猜想】甲认为只有铜;乙认为是铜和铁的混合物;丙认为是铜、铁、锌的混合物。
【交流讨论】大家一致认为丙的猜想不合理,其理由是_____________________________________________________。
【实验与结论】同学们通过实验确定乙的猜想是正确的。请填空:

(4)在实验室称取20 g赤铁矿样品置于玻璃管中,称得样品和玻璃管的总质量为70 g,通入足量CO后加热使样品充分反应(杂质不参与反应),冷却后称得玻璃管和剩余固体的总质量为65.2 g。试计算样品中Fe2O3的质量分数。
答案

知识点:实验探究 金属与金属材料 有关化学方程式的计算
(1)铁在空气中锈蚀,实际上是铁与空气中的水蒸气和氧气等物质相互作用的结果;日常生活中可采用涂油、刷漆等措施进行防锈。
(2)A.根据元素周期表中的信息,金元素属于金属元素,A错误;
B.金原子的相对原子质量取197,质子数为79,根据相对原子质量=质子数+中子数可知,金原子的中子数为118,B错误;
C.原子的核外电子数等于质子数,所以金原子的核外电子数为79,C错误;
D.金元素位于第六周期第IB族,D正确;也可根据排除法,A、B、C均错误,D正确。故选D。
(3)【交流讨论】锌的金属活动性强于铁,铁不能从锌的化合物中置换出锌,即固体中不可能有锌。
【实验与结论】根据乙的猜想是正确的,即滤纸上的物质铜和铁的混合物,因为铁可以与酸发生反应,所以可以向固体中滴加适量的稀盐酸或稀硫酸;现象:有气泡产生,且溶液由无色变为浅绿色;发生反应的化学方程式为Fe+2HCl=FeCl2+H2↑或Fe+H2SO4=FeSO4+H2↑。
(4)反应前后,质量减少了70 g-65.2 g=4.8 g,减少的质量其实就是氧化铁中氧元素的质量,结合氧化铁中氧元素的质量分数,可以求出氧化铁的质量,进而得出氧化铁在样品中的质量分数。
略









