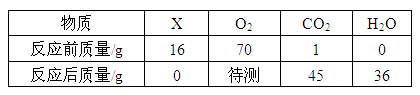
某密闭容器中有X、氧气和二氧化碳三种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表。根据表中信息,判断下列说法正确的是( )
- A.该反应为分解反应
- B.X中含有碳、氢、氧三种元素
- C.生成的CO2和H2O的分子个数比为1:2
- D.反应生成的CO2和H2O的质量比为45:36
答案
正确答案:C
知识点:质量守恒定律及其应用
质量守恒定律表格题的一般解题步骤为:①求待测值;②判断反应物和生成物;③结合选项分析。根据质量守恒定律可知:反应前后物质的质量总和相等,则16+70+1+0=0+“待测”+45+36,求得“待测”=6。
A.要判断反应类型,需判断反应物和生成物。根据“反应前后质量减小的是反应物,质量增大的是生成物”,判断出X、O2为反应物,CO2、H2O为生成物,不符合分解反应的特点,A错误。
B.由以上分析可知,X、O2为反应物,CO2、H2O为生成物,根据反应前后元素种类不变可知,X中一定含有碳、氢元素。
生成物二氧化碳中氧元素的质量为![]() ;水中氧元素的质量为
;水中氧元素的质量为![]() 。生成物中氧元素的质量共有32 g + 32 g=64 g,故反应物中氧元素的质量共为32g,因为反应物中氧气的质量为70g-6 g=64 g,故该化合物中不含氧元素,B错误。
。生成物中氧元素的质量共有32 g + 32 g=64 g,故反应物中氧元素的质量共为32g,因为反应物中氧气的质量为70g-6 g=64 g,故该化合物中不含氧元素,B错误。
C.由以上分析可知,该反应可表示为xX+yO2=zCO2+wH2O,CO2和H2O在反应前后的变化量分别为44g、36g,则参加反应的CO2和H2O的质量分别为44 g、36g。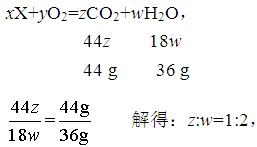
C正确。
D.根据表中数据,CO2和H2O在反应前后的变化量分别为44g、36g,则反应生成的CO2和H2O的质量比为44g:36g=11:9,D错误。
故选C。
略








