有关NaOH与CO2反应的探究如下。
探究一:检验NaOH固体样品露置于空气中一段时间后的成分。
(1)检验样品是否变质。
写出检验样品成分中是否含碳酸根的实验方法(操作、现象及结论)。
(2)检验样品是否完全变质。
实验操作:取样品加水溶解,先加过量的 (填编号),再滴加 (填编号)。
A.盐酸B.KCl溶液C.BaCl2溶液D.Ba(OH)2溶液E.酚酞溶液
探究二:用NaOH溶液测定空气中酸性气体(CO2、SO2)的体积分数。
如图所示,向细玻璃管内注入少量水,形成一段水柱,经检查该装置气密性良好。已知细玻璃管单位长度的容积为0.1mL•cm-1,水柱的质量忽略不计。
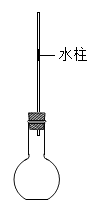
保持外界条件不变,完成以下操作:
①将40mL浓NaOH溶液迅速倒入烧瓶内,立即塞紧橡皮塞,并在细玻璃管上标记水柱底部的位置。
②观察并测量得出水柱缓慢向下移动的距离为2.0cm。
③实验结束后,根据①中的标记,测得该标记以下细玻璃管及烧瓶的总容积为340mL。
(3)写出判断该装置气密性良好的实验现象。
(4)仅根据本次测量数据,该气体样品中酸性气体的体积分数为 (精确到0.001%)。
(5)在上述操作步骤②中,若装置温度略有升高,实验结果 (填“偏大”、“偏小”或“不变”)。
答案
(1)取少量该样品,加入足量的稀盐酸,若有气泡产生,将生成的气体通入澄清石灰水,石灰水若变浑浊则说明样品中含有碳酸根(6分)。
(2)C(2分),E(2分)。
(3)将图中装置直立于桌面一段时间后,如果水柱的位置不发生移动,则说明装置气密性良好(3分)。
(4)0.067%(4分)。
(5)偏小(4分)。
探究一:(1)要想检验样品成分中是否含碳酸根,可以加入某种试剂,使其与碳酸根反应产生气体或沉淀,进而观察到明显现象。可以根据含有碳酸根离子的物质与稀盐酸反应生成CO2来设计实验:取少量该样品,加入足量的稀盐酸,若有气泡产生,将生成的气体通入澄清石灰水,石灰水若变浑浊则说明样品中含有碳酸根。
(2)检验样品是否完全变质,关键是检验其中是否还有NaOH存在,可先加入过量的BaCl2把Na2CO3消耗完全,然后用酚酞溶液检验NaOH是否存在,注意不能选择Ba(OH)2,因为Ba(OH)2会与Na2CO3反应生成NaOH,干扰原样品中NaOH的检验。
探究二:(3)检查如图所示装置气密性的操作方法:将图中装置直立于桌面一段时间后,如果水柱的位置不发生移动,则说明装置气密性良好。
(4)NaOH溶液可以吸收酸性气体(CO2、SO2),样品中酸性气体的体积为2.0cm×0.1mL•cm-1=0.2mL,因此该样品中酸性气体的体积分数为![]() 。
。
(5)温度升高会使气体体积膨胀,使得水柱向下移动的距离偏小,造成测得的酸性气体的体积偏小,故实验结果偏小。
略








