1编号:62794题型:填空题测试正确率:0%
学习了MnO2对过氧化氢溶液(双氧水)分解有催化作用的知识后,某兴趣小组的同学进行了有关“影响过氧化氢分解速率的因素有哪些”的探究。
[探究一]兴趣小组进行了四个实验,实验数据如表:

(1)通过实验1和2对比可知,过氧化氢分解速率与____有关;通过实验____和____对比可知,过氧化氢分解速率与温度有关,且温度越高,分解速率越____(填“快”或“慢”)。
(2)用35mL质量分数为30%的过氧化氢溶液制取氧气,为了减小反应速率,加了一定量的水稀释,这会使产生氧气的总质量____(填“减小”、“不变”或“增大”)。
[质疑]CuO能否起到类似MnO2的催化剂作用呢?于是,小组同学又进行了以下探究。
[探究二]猜想一:CuO不是催化剂、也不参与反应,反应前后____和____不变;
猜想二:CuO参与反应产生O2,反应前后____和____改变;
猜想三:CuO是反应的催化剂,反应前后____和____不变。
[实验]用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如图实验:

(3)填写如表:

将表中需要填写的内容填写到下列横线上:
(a)____;(b)____;(c)____。
(4)步骤①的目的是与步骤____(可直接填阿拉伯数字)作对比,检验加入氧化铜后过氧化氢的分解速率是否有改变。
(5)步骤④需用到的实验仪器和用品有:铁架台(带铁圈)、漏斗、烧杯、滤纸、____。
2编号:62793题型:填空题测试正确率:0%
2013年12月2日,我国“嫦娥三号”探测器由长征三号运载火箭发射,首次实现月球软着陆和月面巡视勘察。“玉兔”月球车底盘和车轮由铝合金材料制成。看见玉兔车金灿灿的车身后,小聪同学想到家里新换的水龙头,从说明书上了解到该水龙头是铜质镀铬,好奇的小聪想探究铬与常见金属铁、铜的活动性强弱,请你一同参加。
(1)知识回顾:金属活动性顺序:K、Ca、Na、Mg、Al、Zn、Fe、Sn、Pb、(H)、Cu、____(填元素符号)、Ag、Pt、Au。
(2)做出猜想:
猜想1:![]() ;
;
猜想2:![]() ;
;
猜想3:____![]() ____
____![]() ____(填元素符号)。
____(填元素符号)。
[查阅资料]
①铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜。
②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
(3)设计与实验
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸。

将表中需要填写的内容填写到下列横线上:铜片表面____(填“有”或“无”)气泡产生,溶液颜色为____色。
(4)结论与解释
小聪得到的结论是:猜想____正确。
(5)知识运用
将铬片投入FeSO4溶液中,反应____(填“能”或“不能”)进行。若能进行,实验现象为溶液由____色变成____色。
3编号:62792题型:填空题测试正确率:0%
据有关资料报导,世界上每年因腐蚀而报废的金属约为年产量的20%~40%。某学习小组在实验室开展了与此相关的探究活动,请仔细阅读并完成下列实验报告。
[查阅资料]碱石灰可以做干燥剂。
[探究目的]探究____锈蚀的条件。
[探究方案]如图所示的是甲、乙两种实验方案(a、b试管中开始盛有的均为经过煮沸的蒸馏水,a试管与大气相通)。

[观察记录]按图甲实验,一周后观察到____(填小写字母序号)装置的液面处铁丝有锈斑,____(填小写字母序号)中无明显变化;按图乙实验,几分钟后就能看到____(填大写字母序号)中铁丝表面变色,而____(填大写字母序号)中无明显变化。
[问题分析]甲方案说明铁生锈是铁与____(填物质名称)和____(填物质名称)共同作用的结果,乙方案不具有甲方案中____(填“a”、“b”或“c”)装置的作用。
4编号:62791题型:填空题测试正确率:0%
认识燃烧,科学地利用和控制燃烧,使燃烧为人类服务是十分重要的,某兴趣小组为探究可燃物燃烧条件进行了如下实验。
[查阅资料]木炭是一种可燃物。
[提出问题]可燃物燃烧需要满足什么条件?
[做出猜想]猜想一:可燃物燃烧需要温度达到可燃物的____;
猜想二:可燃物燃烧需要____(填物质名称)。

[进行实验]某兴趣小组用上图所示的装置进行了实验。在完成气密性检查后填装药品,并已在整个装置中充满了氮气。实验过程中没有拆装仪器,请你参与完成后续的实验,并按要求填表。

将表中需要填写的内容填写到下列横线上:
①____;②____;③____;④____;⑤____;⑥____。
[实验结论]通过步骤____和____的对比,说明猜想一成立;通过步骤____和____的对比,说明猜想二成立。
5编号:62784题型:填空题测试正确率:0%
在实验探究课上,老师给同学们一包红色粉末,该粉末是铜粉和氧化铁粉末中的一种或两种。同学们为确定该粉末的成分,进行如下探究。请回答下列问题。
[查阅资料]金属氧化物能够溶于稀酸;铜不溶于稀酸。
[提出问题]红色粉末成分是什么?
[猜想假设]
猜想1:红色粉末是____(填物质名称);
猜想2:红色粉末是氧化铁;
猜想3:红色粉末是铜和____(填物质名称)的混合物。
[设计方案]取少量红色粉末放入硬质玻璃管中,____(填字母序号),充分反应并观察现象(实验装置如图所示)。
A.先通入一段时间的一氧化碳,然后再点燃酒精灯加热
B.先点燃酒精灯加热一段时间,然后再通入一氧化碳
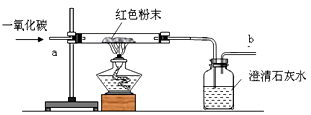
请你完成下表:

将表中需要填写的内容填写到下列横线上:
①____;②____;③____;④____;⑤____。
[实验结论]同学们进行了实验并经过分析,确认猜想3成立。
[反思评价]请你用另一种反应原理证明猜想3成立,实验方案是取少量红色粉末于试管中,加入足量的____充分反应,试管底部有____色固体剩余,溶液变为黄色,则猜想3成立。
6编号:62783题型:填空题测试正确率:0%
7编号:62782题型:填空题测试正确率:0%
课本上测量空气中氧气体积分数的实验装置存在不少的缺点,如污染环境、误差较大等。小明同学在老师指导下,利用铁锈蚀原理测量空气中氧气的体积分数。
[查阅资料]脱氧剂的主要成分为铁粉、少许活性炭、少量氯化钠和水。活性炭是一种载体,可以使脱氧剂中各组分混合均匀,并使铁粉疏松、透气。
[实验原理]铁生锈消耗集气瓶中的____(填物质名称),生成固态的铁锈,使集气瓶内压强____(填“增大”或“减小”),在压强差的作用下,量筒内水进入集气瓶;氯化钠可以加快铁锈蚀的速率。
[实验过程](1)取一个集气瓶,其实际容积是150mL,取一个量筒,内盛100mL的水。
(2)室温时,将一定量的脱氧剂悬吊在橡皮塞上,再将橡皮塞旋紧到集气瓶口,然后将导气管插入量筒内(如图所示),观察现象。
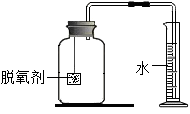
(3)当量筒内水面高度不再变化,且温度恢复至室温时,读出水面在73mL刻度处。
[实验结果]由上述实验数据可以算出,空气中氧气的体积分数是____%。
[反思拓展]本实验的测量结果与理论值不一致,原因可能是____(填字母序号)。
A.使用了足量的脱氧剂
B.脱氧剂中有部分铁粉在实验前已被氧化
C.脱氧剂中的内层的铁粉没有与氧气接触
8编号:62781题型:填空题测试正确率:0%
天然气的主要成分是甲烷(CH4),化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,请你参与探究:
甲烷在氧气中燃烧后生成哪些物质?含碳元素的物质在氧气中完全燃烧生成CO2,不完全燃烧生成CO;无水CuSO4(白色)遇水变蓝色。
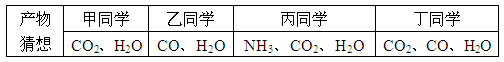
你认为____同学的猜想是错误的。为了验证上述猜想与假设,将甲烷在一定量的氧气中燃烧的产物依次通过如图装置:
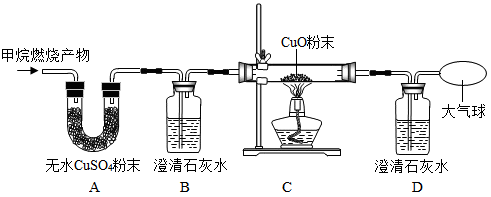
(1)A、B装置的顺序____(填“能”或“不能”)颠倒,若颠倒,将影响产物____(填物质名称)的检测。
(2)实验中用纯净氧气而不用空气的原因是空气中含有____(填物质名称)和____(填物质名称)。
(3)实验中观察到A中无水CuSO4粉末由____色变为____色,B中澄清石灰水____(填“变”或“不变”)浑浊,C中____色粉末变成光亮的____色,D中澄清石灰水____(填“变”或“不变”)浑浊,由此推断丁同学猜想成立。
9编号:62780题型:填空题测试正确率:0%
背景:市场上销售的豆腐干、盐水鸭等食品,常采用真空包装,即将食品装入包装袋,抽出包装袋内的空气,再充入防止食品变质的气体,然后封口。真空包装的目的是除去空气使大多数微生物因缺少____(填物质名称)生命活动受到抑制,停止繁殖,从而防止食品变质。
[提出问题]充入食品包装袋中的气体是什么?
[猜想假设]同学们经过激烈讨论,最后提出了气体可能有三种情况:①N2;②CO2;③H2。
[提出方案](1)小明同学认为气体不可能是H2,因为它具有____性。
(2)为了继续探究气体的成分,小华和小红两位同学各提出了一种方案。
①小华方案:收集一瓶该气体,把一根燃着的木条伸入瓶中,发现木条熄灭。由此得出气体是CO2。该方案是否可行?____(填“是”或“否”)。
②小红的方案被同学们认可。走进食品生产工厂,在装有该气体的容器(容器内压强接近大气压)上连接了如图的装置。
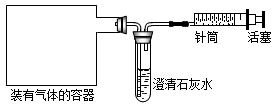
a.为了使容器内的气体通过澄清石灰水,活塞应向____(填“左”或“右”)移动。
b.不管气体是CO2还是N2,试管中都有的实验现象是导管口有____产生。
c.经过实验后,发现澄清石灰水变浑浊,证明气体是____(填物质名称)。